打破学科壁垒!多中心联手在早产儿健康研究领域取得突破
2月27日,南方医院儿童中心副主任医师沈薇作为共同第一作者兼通讯作者,联合珠江医院何彦、周宏伟团队及深圳市儿童医院新生儿科黄为民团队,在早产儿健康研究领域取得重大突破,成功揭示了肠道菌群发育对早产儿晚发型败血症(LOS)的影响机制。
聚焦临床痛点,开启跨域协作
早产儿由于器官和免疫系统发育不成熟,极易发生感染,其中LOS是导致死亡和远期神经发育障碍的主要原因之一。然而,其发病机制复杂,传统的诊断方法敏感性和特异性有限,临床仍缺乏有效的早期预警指标和干预靶点。
面对这一挑战,研究团队在CALM平台框架下,由南方医院儿童中心牵头,联合珠江医院、深圳市儿童医院,自2021年起组建“早产儿肠道菌群多中心队列”(CALM2005队列),共同推进队列建设与样本收集,并得到广州市妇女儿童医疗中心、佛山市妇幼保健院等分中心积极响应。多中心团队兼具丰富临床资源、成熟基础研究平台及领先微生态检验分析技术等几大优势,多方强强联合,形成了从队列构建、数据分析到机制探索的完整研究链条。
构建“菌龄”量化评估系统,解码晚发型败血症新机制
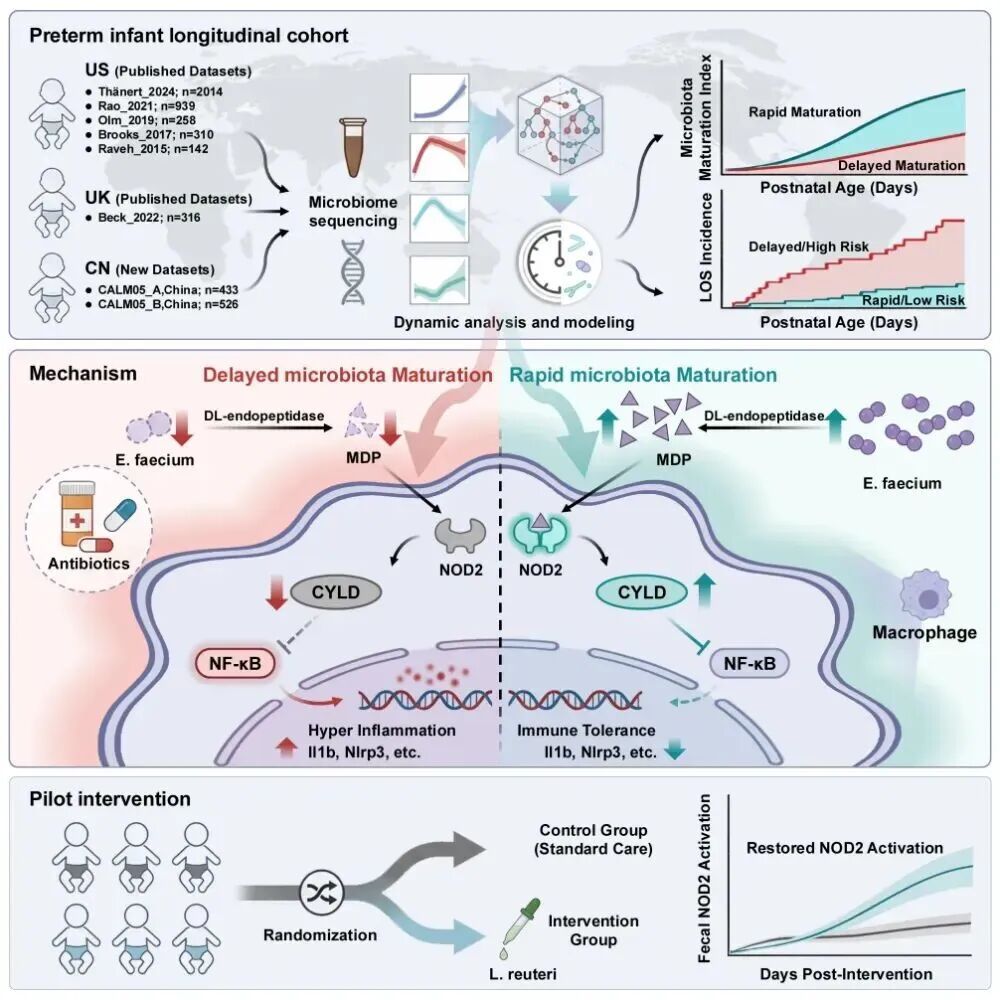
该研究基于CALM2005队列,联合分析中、美、英三国8个临床队列共4938份纵向粪便样本,针对早产儿菌群地域差异及高度动态特征,利用机器学习构建量化早产儿肠道发育速率的“菌群年龄”模型。结果证实,菌群发育迟缓是LOS发生的独立风险因子,其预测稳健性优于任何单一细菌特征;中介效应分析显示,抗生素暴露诱发的败血症风险中,约36%通过诱导菌群发育迟缓介导,为“抗生素暴露增加败血症风险”的临床现象提供了肠道菌群发育维度的科学解释。
在探究发育迟缓的生物学功能时,研究通过宏基因组学分析及动物实验鉴定出关键功能酶——DL-内肽酶(主要来源于屎肠球菌),其可水解肽聚糖并释放胞壁酰二肽(MDP)。MDP作为宿主模式识别受体NOD2的天然配体,可调控肠道免疫信号激活水平。在菌群发育较快的早产儿中,持续的MDP信号激活NOD2受体并上调巨噬细胞负性免疫调节因子CYLD,进而抑制NF-κB通路过度激活,限制内毒素诱导的炎症反应,促进免疫耐受形成;而在抗生素暴露导致的菌群发育迟缓使该免疫训练过程缺失,宿主在面对病原体挑战时更易出现失控的过度炎症反应。
基于DL-内肽酶—MDP—NOD2轴促进免疫耐受降低晚发型败血症风险的新机制,团队在南方医院开展随机对照试点试验(RCT),纳入15例早产儿(5例干预、10例对照),干预组口服补充高DL-内肽酶活性的罗伊氏乳杆菌(L. reuteri DSM 17938)后,患儿粪便NOD2激活水平显著提升,在分子层面部分修复了抗生素诱导的免疫信号缺失,且14天干预期内未观察到感染或坏死性小肠结肠炎等不良事件,提示良好安全性。
跨域协作引领医学创新
这项汇聚多单位、多学科智慧的研究,围绕早产儿晚发型败血症(late-onset sepsis,LOS)这一新生儿重症领域关键难题,揭示了生命早期菌群发育的演替规律及其临床意义,为新生儿重症监护病房(NICU)开展精准菌群监测及基于免疫耐受诱导的防治策略提供了理论依据。研究成果在知名学术期刊Cell Host & Microbe在线发布:《Gut microbiota immaturity with DL-endopeptidase deficiency links antibiotic use to preterm late-onset sepsis》。
这项研究的成功离不开多中心的紧密协作和多学科的交叉融合。跨域协作的联合研究模式是攻克复杂医学难题的有效途径,科研团队表示,将进一步加强与兄弟单位的合作,推动新生儿医学领域的创新发展。
在医学科学飞速发展的今天,单一单位、单一学科的研究模式已难以应对复杂的医学问题。只有打破学科壁垒,加强单位间的协作与交流,整合优势资源,才能实现医学研究的跨越式发展。南方医院、珠江医院与深圳市儿童医院的联合研究,为早产儿晚发型败血症的研究开辟了新的方向,也为跨单位、跨学科的医学研究提供了成功范例。

