

上世纪五十年代,Th. Förster等人在高浓度芘分子溶液中发现了激基缔合物。时至今日,以激基缔合物为工作物质的激光器已经在现代工业中扮演着重要角色。但由于激基缔合物形成的浓度依赖性,在保证良好生物相容性的前提下,利用激基缔合物荧光进行生物成像的分子探针仍然较少。近期,Science杂志报道了超分子网络中的金纳米团簇在低浓度下形成激基缔合物(Science,2016,353, 571-575),但如何诱导超分子组装体中的有机荧光团在较低浓度下,特别是在生物环境中形成激基缔合物仍然是一个挑战。
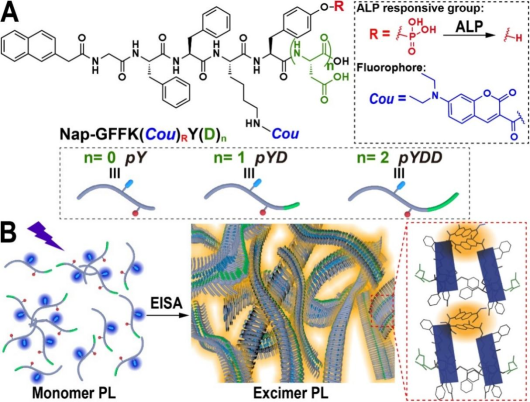
近期,一种通过酶促自组装纳米纤维使荧光团在低浓度下和生物环境中形成激基缔合物的策略被提出,相关研究成果以Enzyme Instructed Self-assembly Enabled Monomer-excimer Transition to ConstructHigher Ordered Luminescent Supramolecular Assembly for Activity-based Bioimaging为题,发表在Angewandte Chemie International Edition上,并且被选为VeryImportant Paper (VIP)。论文第一作者为我院研究生钟远智,通讯作者为我院特聘教授杨志谋教授,蔡延滨副教授及战捷博士。
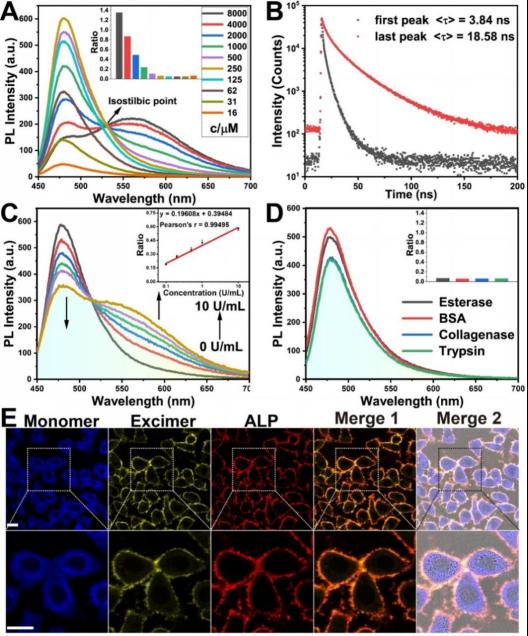
该研究将香豆素染料通过共价键连接到碱性磷酸酶(ALP)响应的小分子多肽上(如pYD),得到的多肽衍生物在低浓度下通过ALP触发的自组装,形成纳米纤维结构,纳米纤维中紧密的分子堆积诱导其中的香豆素形成激基缔合物。进一步研究发现,设计的短肽衍生物在高表达ALP的细胞膜或肿瘤组织中原位自组装形成发光纳米纤维,能够实现高效记录内源性ALP的时空分布细节。
在ALP处理前,pYD中的香豆素仅在高浓度时(如4 mM)才能形成激基缔合物。在ALP的作用下,较低浓度(如125 μM)的pYD自组装成纳米纤维并形成即可促进香豆素激基缔合物的形成,且pYD可以选择性地、定量地、快速地响应于外部的或细胞内源性的ALP。
此外,在细胞分裂末期会形成细胞间桥,利用细胞间桥膜上的ALP,pYD发生原位自组装并发出香豆素激基缔合物荧光,而香豆素的单体荧光穿过了细胞间桥中致密的中体,表明pYD可作为细胞间桥的分子成像探针。利用肿瘤细胞与正常细胞内源性ALP活性的差异,pYD可以有效鉴别出肿瘤细胞,且在肿瘤细胞与正常细胞共培养的条件下也不影响pYD对肿瘤细胞的识别。在荷瘤裸鼠中,高表达ALP的肿瘤组织比正常组织显示出更高的信号响应能力,使pYD能够快速的富集在肿瘤组织实现肿瘤显影,提示该酶促自组装激基缔合物荧光探针有望成为癌症早期诊断的潜在策略。
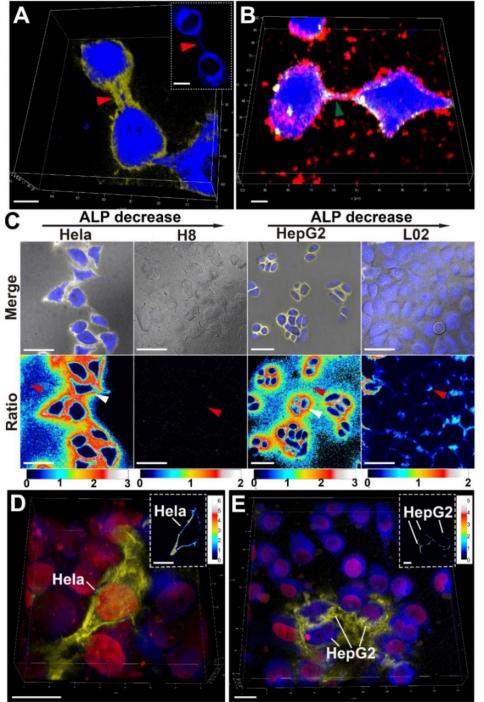
总之,该工作利用超分子自组装在较低浓度下诱导有机荧光团激基缔合物的形成,并赋予了激基缔合物以超分子组装体的生物成像特性。该工作为超分子化学与激基缔合物的结合提供了思路,同时也为开发基于激基缔合物的分子探针提供了思路。
论文信息:
Enzyme Instructed Self-assembly Enabled Monomer-excimer Transition to Construct Higher Ordered Luminescent Supramolecular Assembly for Activity-based Bioimaging
Yuanzhi Zhong, Jie Zhan,* Guanghui Xu, Yumiao Chen, Qin Qin, Xu Liao, Shaodan Ma, Zhimou Yang,* and Yanbin Cai*
Angewandte Chemie International Edition
DOI: 10.1002/anie.202014278