当前位置: 研招首页 > 正文
多项研究新进展为骨关节炎转化治疗提供新策略
近日,珠江医院临床研究中心丁长海教授团队在骨关节炎(Osteoarthritis, OA)研究领域连续取得新进展,为OA的发病机制解析及转化治疗提供了创新性策略,标志着该团队在OA基础与转化研究领域迈入新台阶。丁长海表示,团队将进一步推进这些成果的临床转化,包括优化纳米药物递送系统、开发靶向乳酸化修饰的小分子抑制剂,以及开展基于工程化干细胞的临床试验,为全球数亿OA患者提供更高效的治疗方案。
DNA纳米机器靶向逆转线粒体功能障碍
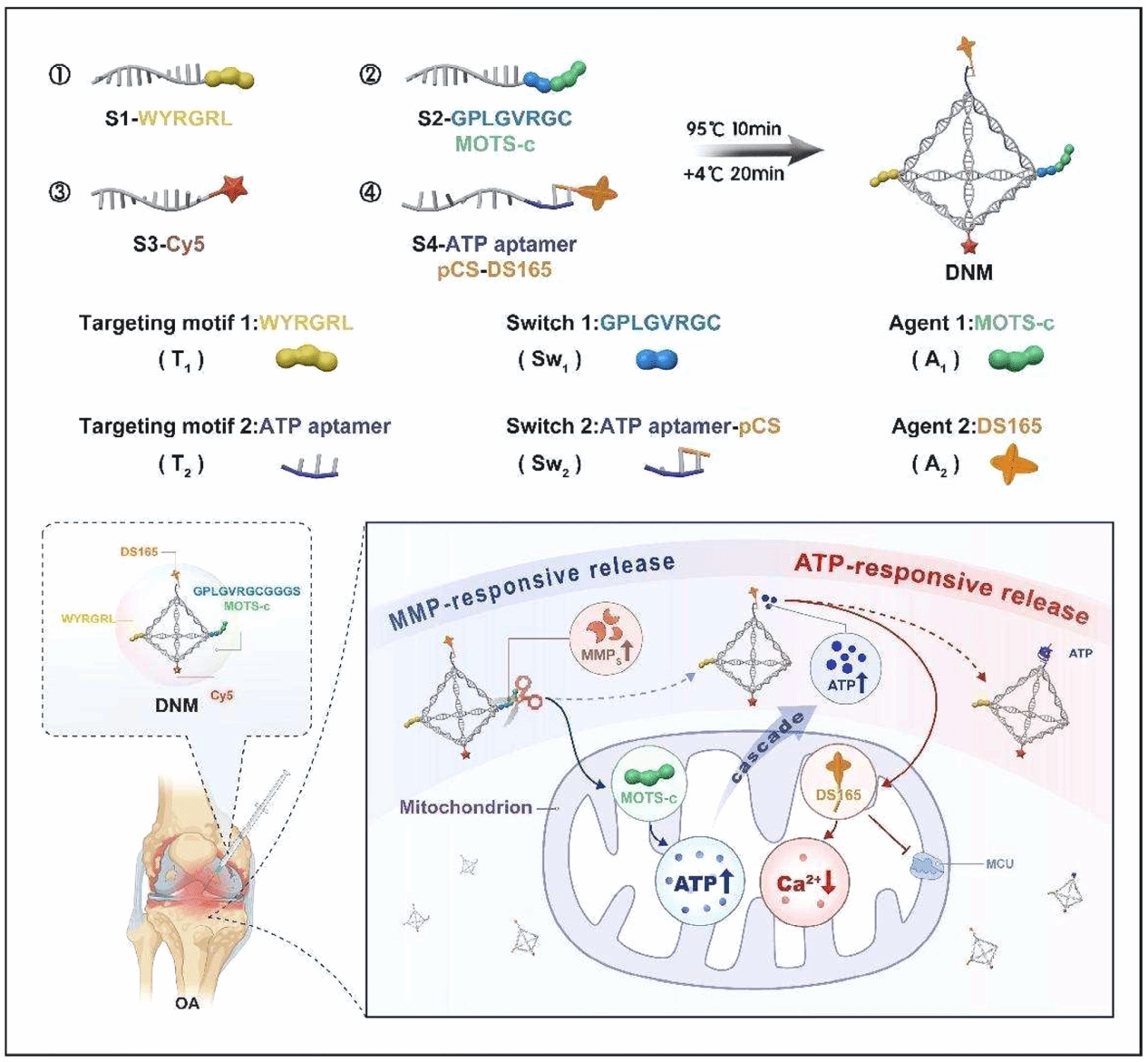
该研究首次构建了一种智能DNA纳米框架载体,通过“双靶向+级联释药”机制精准干预软骨细胞线粒体功能。
研究发现,OA微环境中线粒体与内质网间钙离子转运失衡是软骨退变的关键诱因。团队设计DNA纳米机器,通过靶向肽段和ATP适配体修饰,实现软骨及线粒体双重靶向;在基质金属蛋白酶和ATP的级联响应下,依次释放MOTS-c和DS165药物,分别激活线粒体代谢功能并抑制钙超载。动物实验表明,该策略显著延缓软骨退变和细胞外基质降解,为OA提供了全新纳米药物治疗方案。
该研究在Advanced Functional Materials发表,题为《A DNA Nanomachine Reverses Mitochondrial Dysfunction by Cascaded Drug Release to Treat Osteoarthritis》。珠江医院薛松、赵洋、黄诗乾、广州市第一人民医院阮光峰为论文共同第一作者;珠江医院丁长海、张超,同济大学张祎男、安徽医科大学第二附属医院胡伟为通讯作者。
UGDH乳酸化修饰调控OA进程新机制
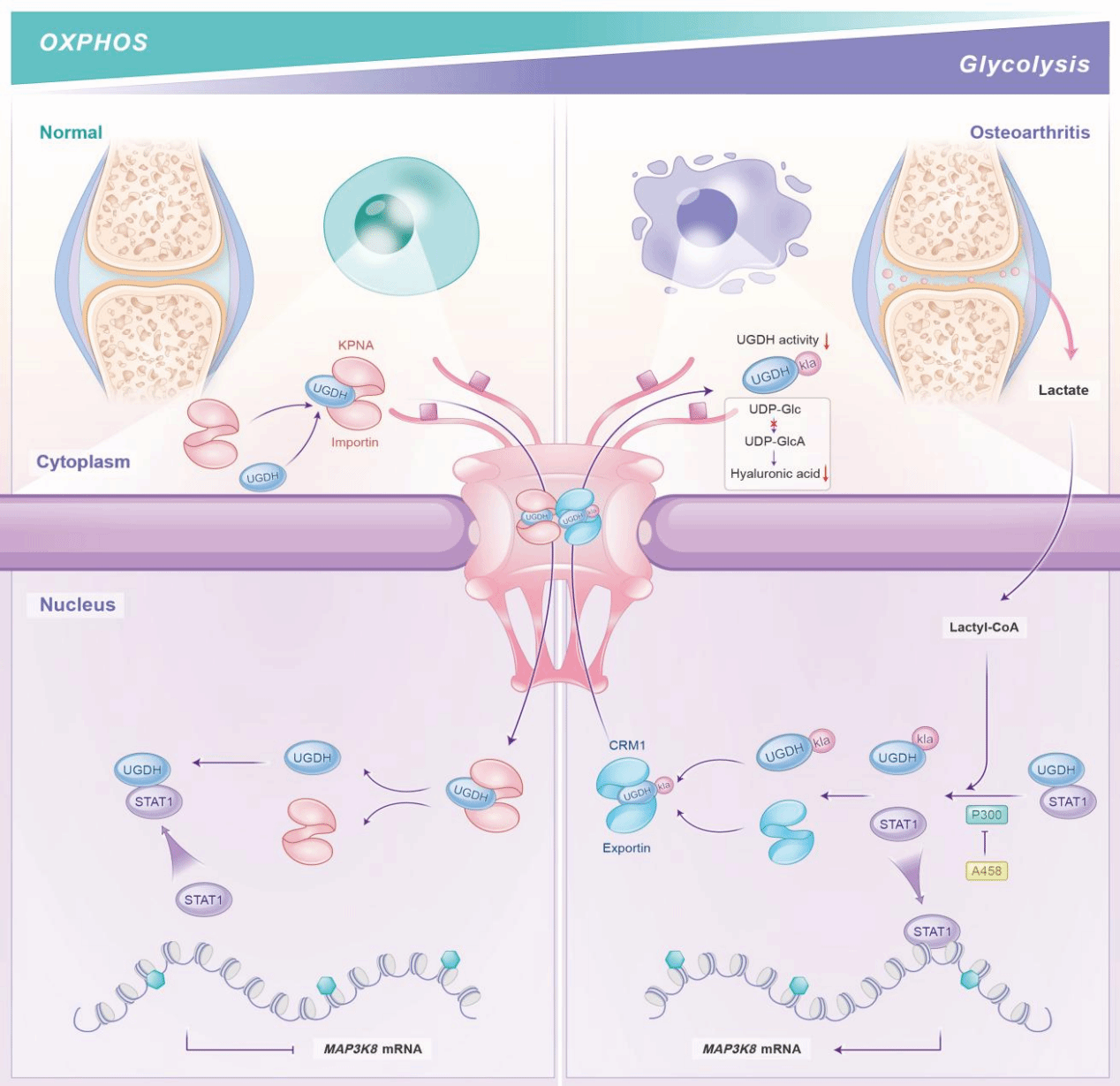
团队首次揭示了代谢重编程驱动的蛋白质乳酸化修饰在OA中的关键作用。通过单细胞测序和临床样本分析,发现OA患者滑液及软骨细胞中乳酸水平异常升高,并伴随UDP-葡萄糖脱氢酶(UGDH)K6位点乳酸化修饰增强。机制研究表明,UGDH乳酸化通过抑制糖胺聚糖合成、调控核质转运并激活MAP3K8-MAPK信号通路,加速软骨降解。研究进一步证实,酰基转移酶P300抑制剂A485可靶向阻断UGDH乳酸化,显著缓解OA进展。该成果为开发靶向代谢修饰的OA治疗药物奠定了重要理论基础。
该研究在Advanced Science发表,题为《UGDH Lactylation Aggravates Osteoarthritis by Suppressing Glycosaminoglycan Synthesis and Orchestrating Nucleocytoplasmic Transport to Activate MAPK Signaling》。珠江医院蓝蔚仁为论文第一作者,珠江医院丁长海、汤苏安为通讯作者。
纳米颗粒与靶向肽双重工程策略增强干细胞治疗效能
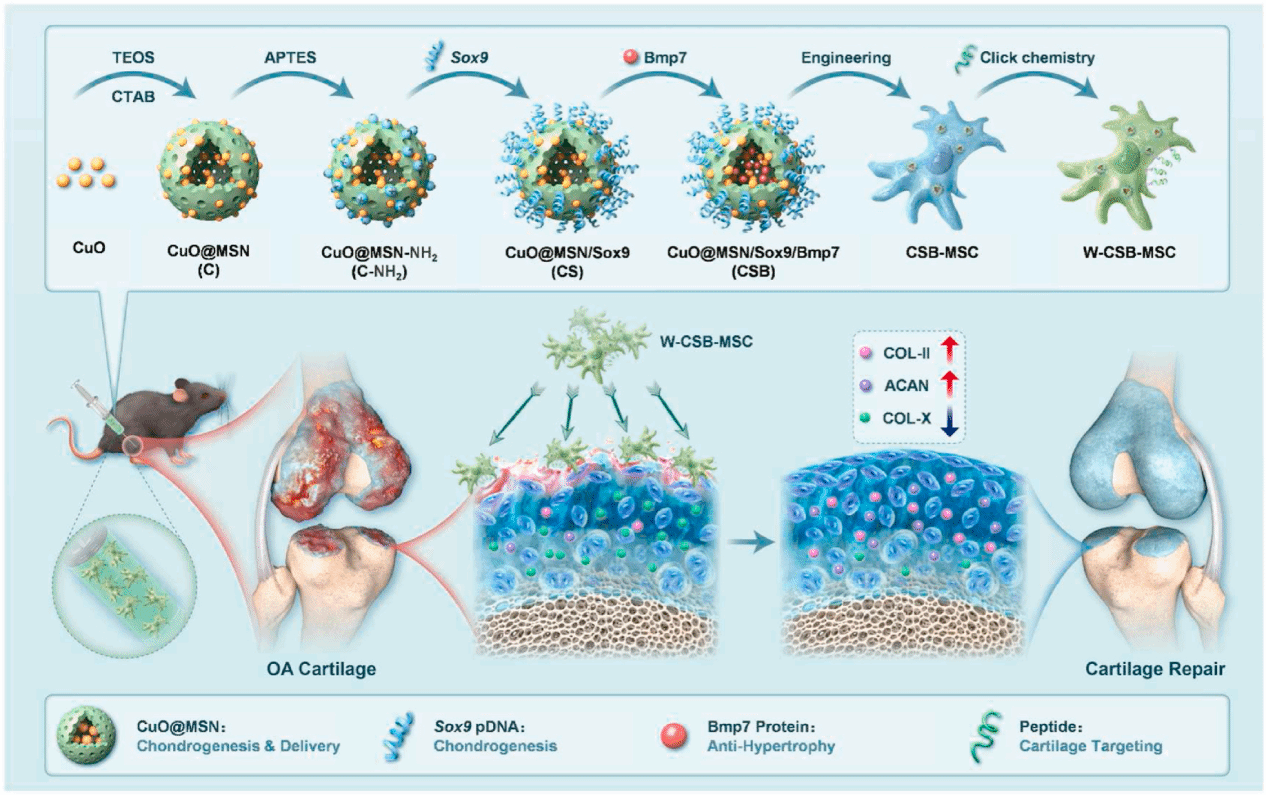
团队创新性开发了一种铜基纳米颗粒(CuO@MSN)与软骨靶向肽(WYRGRLCCCC)双重修饰的间充质干细胞(MSCs)工程策略。该纳米颗粒可递送Sox9基因和Bmp7蛋白,分别促进MSCs软骨分化并抑制肥大化;靶向肽修饰则显著提升MSCs在关节腔和软骨组织的驻留能力。动物实验及临床OA患者软骨样本验证显示,双重修饰的MSCs可高效促进透明软骨再生,减少血管化和钙化。该研究为干细胞治疗OA的临床转化提供了关键技术支撑。
该研究在Biomaterials发表,题为《Efficiently directing differentiation and homing of mesenchymal stem cells to boost cartilage repair in osteoarthritis via a nanoparticle and peptide dual-engineering strategy》。珠江医院吴翠茜、黄振文为论文共同第一作者,珠江医院丁长海、韩卫雨、陆遥为通讯作者。