

流感病毒(Influenza virus)频繁变异引发的耐药性及重症感染中“细胞因子风暴”是临床治疗的重大挑战。临床亟需能同时高效抑制病毒复制并精准调控过度炎症反应的单一药物,以简化方案、降低风险、提高疗效。近期,南方医科大学药学院刘叔文教授团队联合华南农业大学宋高鹏教授团队,基于“病毒-宿主”多功能协同抗病毒新策略,对天然产物齐墩果酸进行结构优化,成功获得可同时靶向PA–PB1与巨噬细胞调控的抗流感病毒新型小分子化合物A5,研究成果以封面文章发表于《Acta Pharmaceutica Sinica B》,并被其发表评述文章(editorial),专门指出A5可能为一个改写流感治疗规则的双靶点抗病毒化合物,论文题为“A novel C-3-substituted oleanolic acid benzyl amide derivative exhibits therapeutic potential against influenza A by targeting PA–PB1 interactions and modulating host macrophage inflammation”。
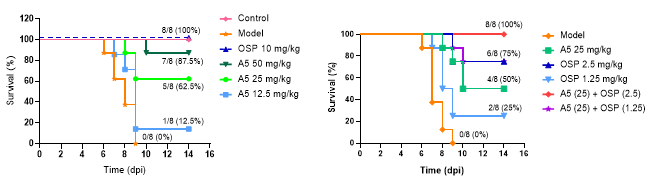
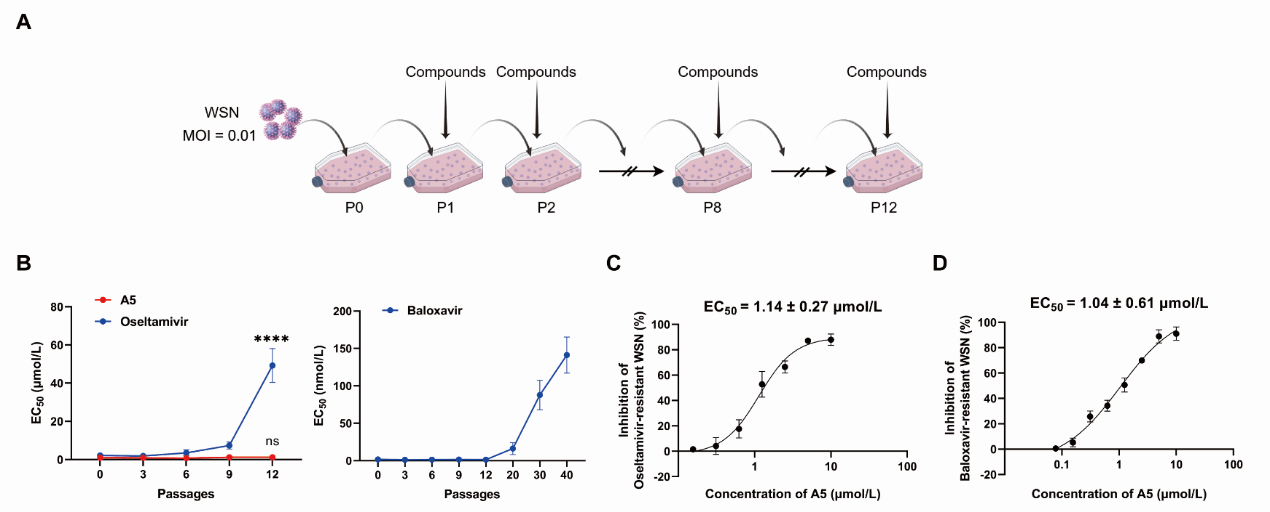
RNA依赖性RNA聚合酶(RdRp)作为病毒复制的核心元件,其PA亚基与PB1亚基的相互作用界面(PAc–PB1N)因其高度保守性被视为理想药物靶点。A5为C-3取代的齐墩果酸苄酰胺衍生物,靶向高度保守的RNA聚合酶PAC结构域,高效抑制病毒PA-PB1亚基相互作用。A5在纳摩尔浓度对多种临床株、奥司他韦耐药株及巴洛沙韦耐药株表现出广谱抗病毒活性(EC50介于0.60 -1.83 μM),并可与奥司他韦协同增效,且具备较高的耐药屏障。同时,A5可调节宿主免疫反应,通过抑制TLR4通路过度激活,减轻甲型流感病毒诱导的巨噬细胞炎症因子释放,在小鼠模型中有效降低病毒载量、缓解病毒性肺炎并提高生存率,且与奥司他韦联用展现出协同抗病毒作用。此外,团队对A5进行了初步的安全性评价,小鼠急性毒性实验200 mg/kg剂量下腹腔注射给药未见明显毒性反应,表明该活性化合物其具有良好的安全窗。
研究基于齐墩果酸骨架进行C-3位精准修饰,获得兼具高效抗病毒与抗炎活性的衍生物,并首次将病毒蛋白互作抑制与宿主炎症通路调控整合于同一分子,突破传统联合用药局限,精准控制病毒复制与过度炎症,为开发兼具直接抗病毒和免疫调节功能的广谱抗流感药物,尤其是针对重症流感的治疗提供新思路。
上述工作获得国家自然科学基金、广东省重大科技专项、广东省药品监督管理局科技创新项目等多项经费资助。南方医科大学在校博士生卢坤玉、何建福与华南农业大学硕士洪崇竣为本文共同第一作者,南方医科大学药学院刘叔文教授、华南农业大学宋高鹏教授与南方医科大学博士后杨婵为共同通讯作者。