

近日,基础医学院病理学系周军团队在Nature Communications上,在线发表了题为” MYG1 drives glycolysis and colorectal cancer development through nuclear-mitochondrial collaboration”的研究论文。
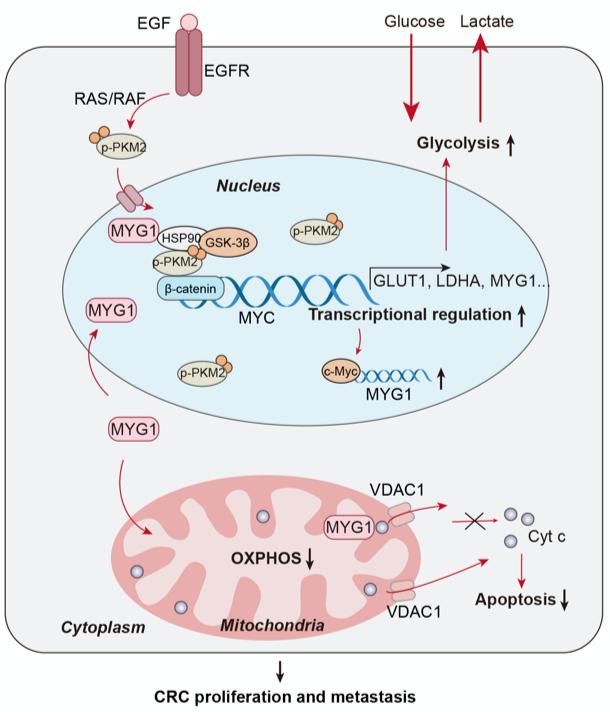
该研究揭示了一种核酸外切酶MYG1(黑素细胞增殖基因1)通过胞核及线粒体不同机制共同调节CRC代谢重编程的新功能,提出MYG1是抑制CRC代谢重塑的潜在靶点。作者利用动物模型、细胞生物学、分子生物学及生物信息学分析方法等技术手段,证实了MYG1在KRAS突变的CRC中表达升高,一方面其通过稳定核内PKM2发挥转录调节作用激活MYC相关的糖酵解基因上调,驱动CRC糖酵;另一方面其在线粒体内抑制线粒体氧化磷酸化功能并抑制细胞凋亡,共同发挥代谢重塑调节功能。该研究表明,MYG1有望成为CRC治疗的重要新靶点,并为理解肿瘤细胞核及线粒体功能上的协同调控提供了新的依据。靶向MYG1可能会扰乱结直肠癌的代谢平衡,并作为结直肠癌诊断和治疗的潜在靶点。
南方医科大学基础医学院周军教授和南方医院郑浩轩教授为本文的共同通讯作者,南方医科大学基础医学院博士生陈建雄、段世玉为本文共同第一作者。
全文链接:https://www.nature.com/articles/s41467-024-49221-0