

近日,基础医学院赵存友教授与曹雄教授团队合作,在精神疾病领域期刊 Schizophrenia Bulletin 发表了题为:Riluzole Restores Circuit and Behavioral Function Altered by Allele-Specific Expression Mediated LINC02449-CPLX1 Dysregulation的研究论文,在分子、神经环路和行为多个层面证明:由等位基因特异性表达(ASE)驱动的脑功能异常,可通过药物实现系统性逆转。
精神分裂症和双相障碍具有显著遗传基础,其复杂致病机制部分来源于非编码调控异常。团队此前通过单卵双胞胎多组学整合分析,鉴定到lncRNA LINC02449 在位点 rs149707223 存在等位基因特异性表达(ASE)失衡,风险等位基因(G)在患者中优先表达,并通过上调突触蛋白 CPLX1,引发前额叶-伏隔核(mPFC–NAc)回路过度兴奋及相关行为异常(Nat Commun,2025;PMID: 41188235)。
在此基础上,本研究构建了AAV介导的LINC02449-G小鼠模型,并给予利鲁唑(Riluzole)干预。结果显示:利鲁唑可剂量依赖性降低Cplx1表达,显著改善社交缺陷与刻板行为,并恢复mPFC–NAc回路异常突触传递(见附图)。
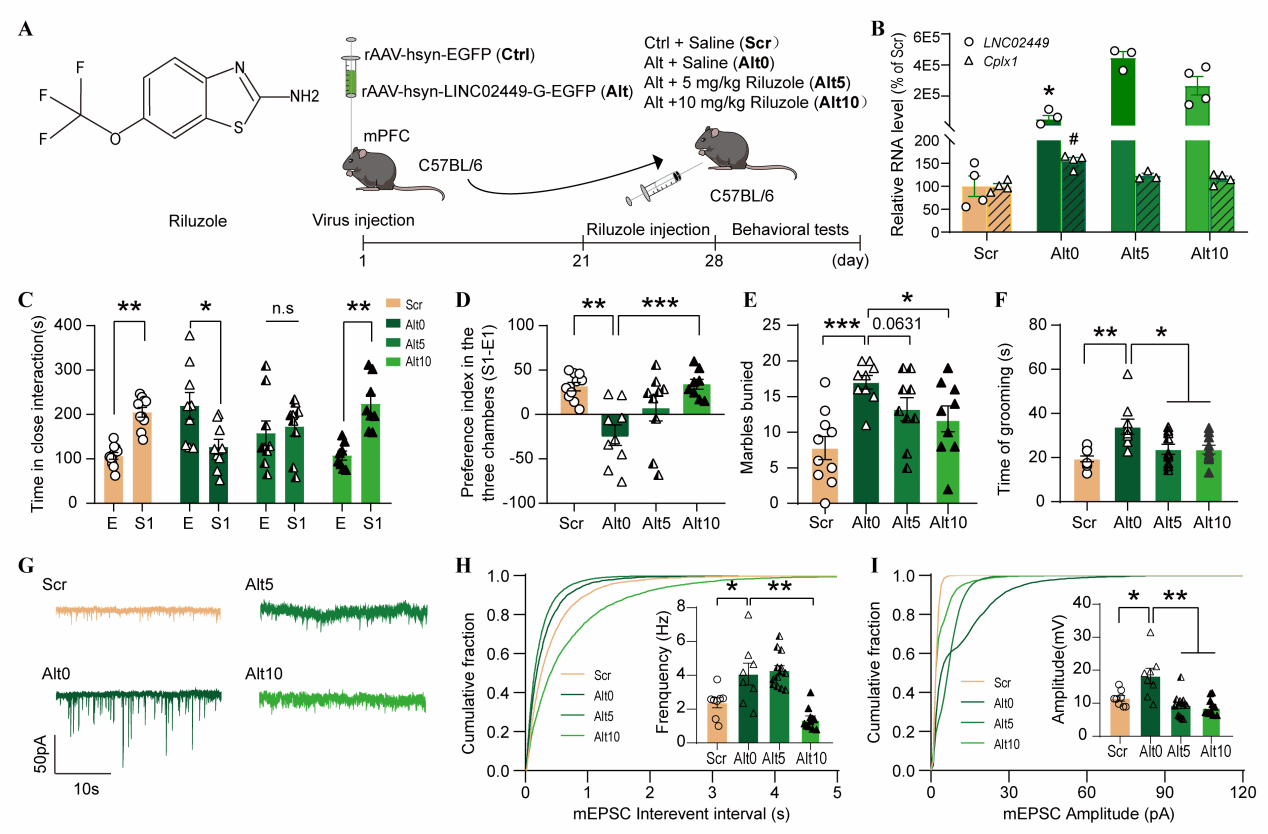
附图 利鲁唑剂量依赖性改善小鼠行为及电生理功能,表现为社交行为恢复及突触传递异常的纠正
综上所述:ASE驱动的lncRNA异常具有药物可逆性,且可通过谷氨酸能调控实现功能恢复。该研究从分子、突触及行为多个层面提供了系统证据,证明非编码RNA介导的遗传调控异常具有明确的干预潜力。本研究将LINC02449–CPLX1致病轴与临床已批准药物利鲁唑建立直接联系,为基于ASE分子分型的精神疾病精准治疗提供了重要的临床前依据,并为“老药新用”策略提供了新的理论支持。
基础医学院博士研究生倪超颖、刘津铭,硕士研究生杨腾飞为本文共同第一作者,赵存友、曹雄为共同通讯作者。
原文链接:https://doi.org/10.1093/schbul/sbag021