

近日,南方医科大学基础医学院病理学系/南方医院病理科梁莉教授团队在Nature Communications(IF=15.7)杂志,发表了题为NEK8 kinase-mediated lactate increase impairs antitumor immunity decreasing radiotherapy sensitivity in colorectal cancer的研究论文,揭示了NEK8通过磷酸化乳酸脱氢酶A(LDHA)促进乳酸生成,抑制CD8⁺T细胞抗肿瘤免疫的新机制,提出增强放疗敏感性和远隔效应的诊疗新靶点及小分子抑制剂。
放射治疗在实现局部肿瘤控制的同时可诱导远端未照射病灶的消退,该现象称为"远隔效应"。然而,临床实践中约30%的结直肠癌患者对放疗产生抵抗,且远隔效应的发生率极低,这成为制约放疗疗效的主要瓶颈。因此,亟需深入解析结直肠癌放疗抵抗及远隔效应的关键调控分子及其作用机制,并发掘相应的干预策略。
近年研究表明:乳酸作为肿瘤细胞糖酵解的重要代谢产物,可以直接分泌至微环境导致肿瘤免疫微环境重塑,影响CD8⁺ T细胞功能。此外,积累的乳酸也可以作为前体物质导致组蛋白赖氨酸发生乳酸化修饰,促进肿瘤演进和免疫逃逸。然而,乳酸如何影响放疗抵抗和远隔效应发生尚不清楚。NEK8作为丝氨酸/苏氨酸激酶家族成员之一,在细胞周期调控、有丝分裂进程、中心体分离、初级纤毛形成及DNA损伤应答等生物学过程中发挥关键作用。然而,NEK8是否影响结直肠癌放疗抵抗及其分子机制尚不明确。
本研究首先构建了小鼠体内结直肠癌放疗耐药模型,经过单细胞测序等多组学数据挖掘与临床队列分析,发现NEK8在结直肠癌中高表达,且其表达水平与CD8⁺ T细胞浸润和放疗敏感性呈负相关性。进一步研究表明:敲除NEK8基因可显著增强放疗侧和远端非放疗侧肿瘤微环境中CD8⁺ T细胞浸润及效应功能,从而提高放疗敏感性并促进远隔效应。在分子机制层面,NEK8与LDHA直接结合,并诱导其Ser196磷酸化,增强LDHA酶活性,促进乳酸生成。乳酸一方面上调MHC-I类基因启动子区的组蛋白乳酸化水平,抑制其表达,影响抗原呈递能力;另一方面分泌至放疗侧肿瘤微环境,甚至通过血液循环进入远端非放疗侧肿瘤微环境,直接抑制CD8+ T细胞的浸润及抗肿瘤活性,从而导致结直肠癌放射治疗抵抗并抑制远隔效应。
基于上述机制,团队进一步通过计算机辅助药物设计开展虚拟筛选,获得了高选择性的NEK8小分子抑制剂CX6258。体内实验结果表明:CX6258与放疗联合应用能够显著抑制原位肿瘤生长及远处转移进展,恢复肿瘤浸润CD8⁺ T细胞的比例与效应功能,有效逆转放疗抵抗,并诱导远隔效应。
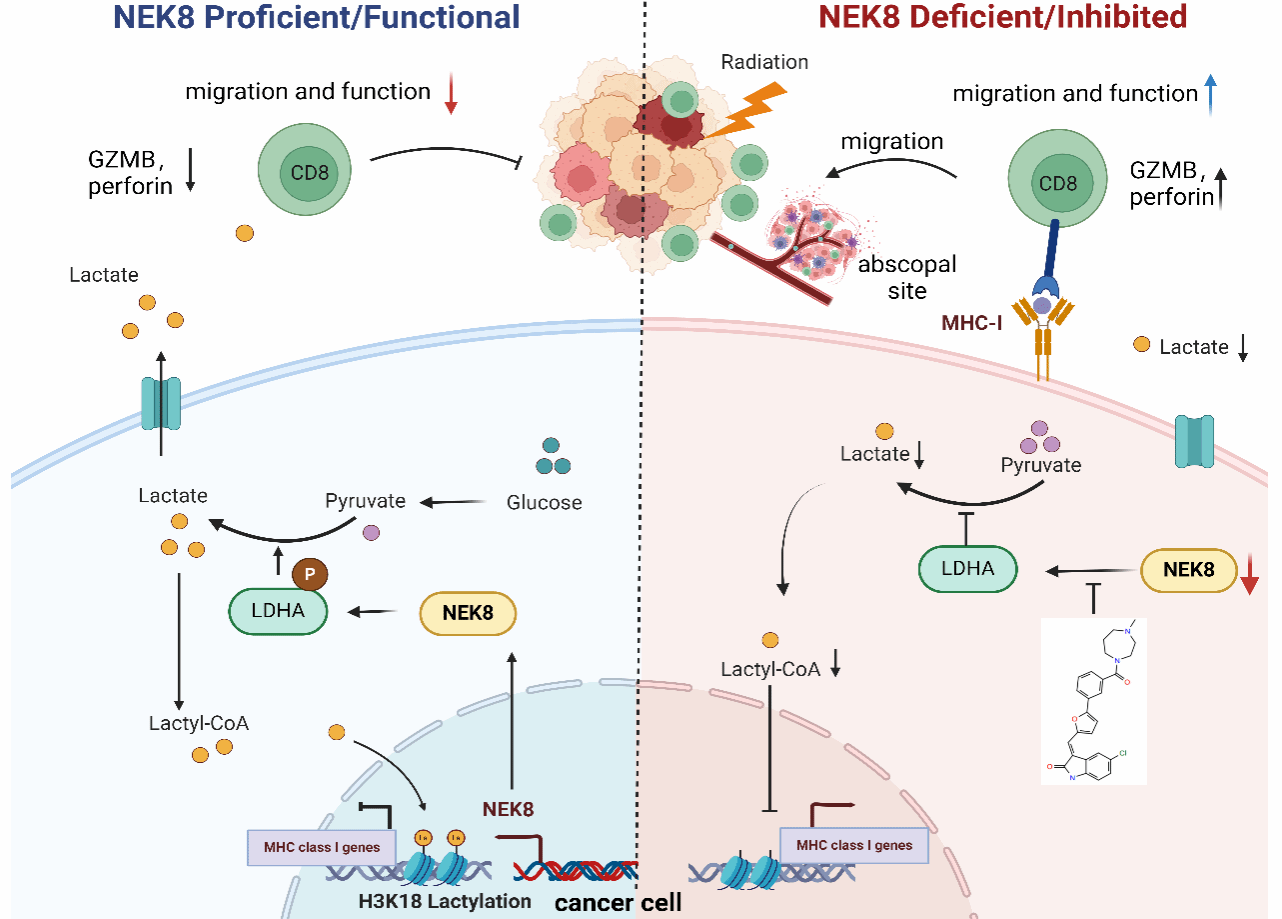
综上,本研究首次明确了NEK8-LDHA-乳酸信号轴在调控结直肠癌放疗免疫应答中的核心作用,研究证实NEK8可作为克服放疗抵抗、诱导远隔效应的新型治疗靶点,其小分子抑制剂CX6258与放疗联合应用展现出显著的协同抗肿瘤效应,为开发结直肠癌精准诊疗策略提供了重要的理论依据与候选药物。
南方医科大学南方医院病理科博士后李明周、南方医院博士研究生倪云飞、基础医学院博士研究生伍杰琼、南方医院博士研究生邹昕为本文共同第一作者,梁莉教授为唯一通讯作者。