

2022年10月4日,Nature Communications在线发表了南方医科大学基础医学院肖东课题组撰写的论文“Autophagy induction promoted by m6A reader YTHDF3 through translation upregulation of FOXO3 mRNA”。该研究首次揭示了m6A阅读器YTHDF3作为营养反应器调节自噬诱导的作用和机制,为RNA转录后修饰通过调控自噬应对营养缺乏应激的范式提供了见解。

自噬是维持细胞内稳态和更新的重要进化机制。自噬的调控对于生命过程至关重要,如自噬参与干细胞特性、胚胎发育、天然免疫和寿命等的调节,而自噬功能障碍可导致癌症发生发展、神经退行性疾病、异常炎症反应、各种代谢紊乱和寿命缩短等。尽管调节自噬的营养传感器已有报道,然而诸如m6A等表观转录修饰在调节饥饿诱导的自噬中的功能尚不清楚。已有的一系列研究揭示了营养缺乏和其它应激反应中表观转录组学的明显动态变化,这提示了这种变化与自噬调节高度相关的可能性。因此,我们推测动态可逆的RNA修饰可响应不断变化的营养信号实现迅速的基因调控,对自噬发挥重要影响,并且一些表观转录组成员在此过程中可能发挥关键作用。
该研究成果揭示了RNA表观转录修饰和自噬调控间的重要联系;所提供的证据表明,m6A阅读器YTHDF3可通过识别METTL3介导的m6A高甲基化发挥营养反应器的作用诱导自噬,其识别FOXO3 mRNA终止密码周围的高m6A修饰,并募集eIFs以促进FOXO3翻译,进一步转录激活自噬相关基因表达,进而促进自噬。此研究揭示RNA甲基化修饰可作为潜在靶点,通过其调控自噬干预某些疾病的进展,例如癌症发生发展或者衰老相关疾病的进程等。
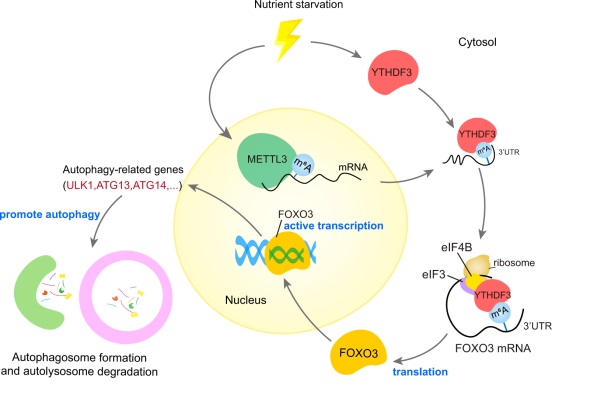
营养应激状态下YTHDF3调控自噬过程的工作模式图
南方医科大学郝伟超博士和奠梅娟博士为本文的共同第一作者,南方医科大学肖东研究员、广东省人民医院孙妍研究员和南方医科大学汪佳宏助理研究员为本文的共同通讯作者。