

近日,基础医学院肿瘤研究所樊俊兵教授团队在Advanced Materials(一区,影响因子29.4)在线发表了题为“Bioinspired Adaptive Microdrugs Enhance the Chemotherapy of Malignant Glioma: Beyond Their Nanodrugs”的研究论文。
胶质瘤是颅内恶性程度最高的原发性肿瘤,患者五年生存率不足5%,其主要原因在于血脑屏障(BBB)的存在使得目前大多数药物难以进入脑部肿瘤组织发挥疗效。多学科交叉融合,利用纳米材料递送药物,提升药物穿越BBB的能力,为胶质瘤治疗带来了新的思路。
自1986年,Matsumura和Maeda等人提出了高渗透性和滞留效应(EPR)以来,其一直被认为是设计纳米药物递送系统的中心法则:即当纳米药物的尺寸足够小时(通常< 200 nm),可通过肿瘤血管中相邻的内皮细胞间隙渗透并滞留在肿瘤组织内。由于BBB的特殊的生理结构,对于胶质瘤药物递送提出了更高的要求,即纳米药物的尺寸越小越好,通常< 100 nm;进一步通过表面修饰提升穿越BBB和药物递送效率。即使如此,纳米药物递送系统穿越血脑屏障的能力仍有待提升。
面对临床问题,向自然学习,寻找解决之道!在生命系统中,如细胞,是具有良好自适应性形变能力的软物质颗粒,当细胞与细胞或细胞与组织界面接触时,除了分子水平的特异性识别,还可以自适应的发生形变,使其能够穿越各种生理屏障,同时这种形变能力可以增加细胞与细胞界面的识别接触,促进细胞间的互作。受此启发,团队在前期研究基础上(Advanced Materials, 2023, 35, 2304187;Nature Communications, 2023, 14, 5575),发展了具有良好自适应形变能力的海藻酸钠微凝胶药物递送系统。结果表明:当赋予药物颗粒良好的自适应形变能力时,微凝胶药物颗粒(0.8 μm-3 μm)能够通过形变进一步增加与内皮细胞和肿瘤细胞间的识别和内吞效率,高效穿越血脑屏障/血脑肿瘤屏障(BBB/BBTB)到达肿瘤组织。同时,仿生自适应性微凝胶药物颗粒比纳米凝胶药物颗粒能携带更多的药物穿越BBB/BBTB,并深层次渗透到肿瘤组织,显著提升了化疗药物在肿瘤部位的递送效率,大大延长了原位胶质瘤小鼠的生存期。
该工作突破了传统脑部药物递送体系尺寸的局限,利用生命系统中自适应形变这一客观存在的自然现象,结合分子水平的特异性识别,显著提升了药物穿越生理屏障和深层次渗透肿瘤组织的能力,并实现了药物在肿瘤部位的高效递送,为胶质瘤治疗提供新的思路。
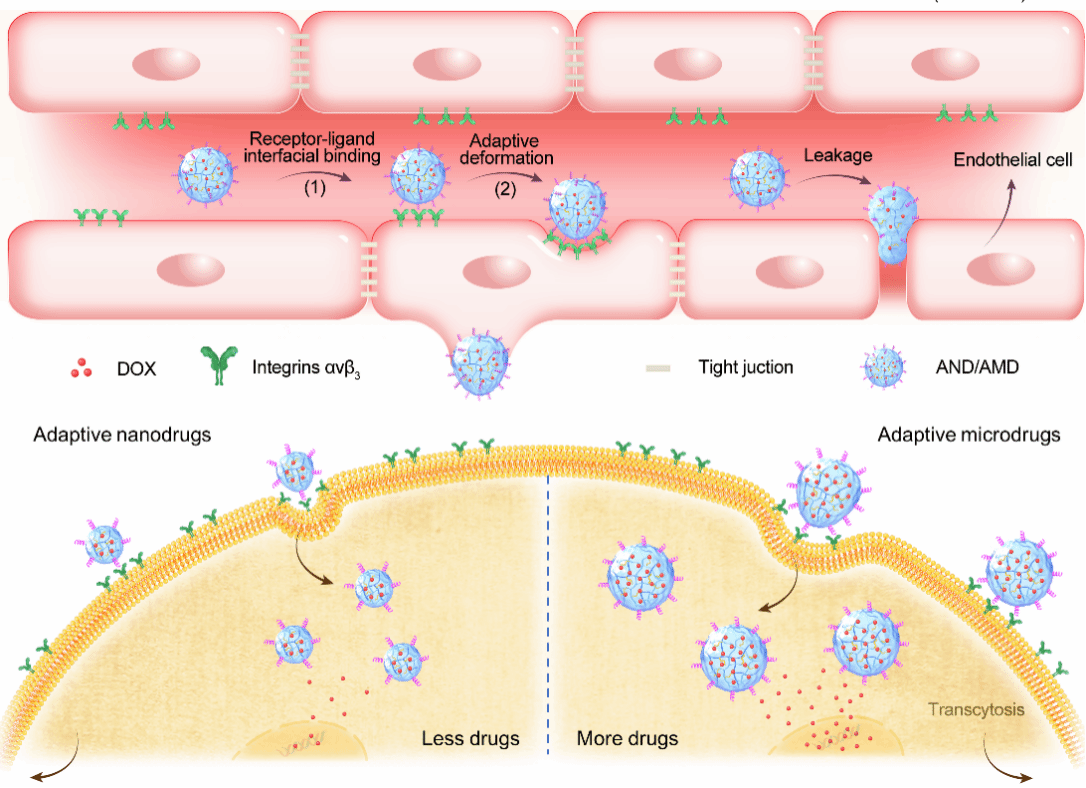
附图 仿生自适应性微/纳米凝胶药物与细胞界面相互作用示意图
基础医学院博士生王学佼为本文第一作者,樊俊兵教授为通讯作者。
全文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202405165