作者: 来源: 阅读量: 发布时间:2022-08-26 11:03:13
由SARS-CoV-2引起的2019年冠状病毒病(COVID-19)已成为全球流行病。目前,针对SARS-CoV-2的疫苗接种是预防这种传染病的关键策略,亟需评估疫苗接种后获得性免疫的有效方法。SARS-CoV-2通过其刺突蛋白中的受体结合结构域(RBD)识别人体细胞表面的血管紧张素转换酶2(ACE2)来入侵细胞,接种疫苗后获得的中和抗体(NAbs)可以竞争性结合RBD从而阻断SARS-CoV-2的入侵。因此,对血清中NAbs水平的检测可以评估疫苗免疫效果并协同指导针对新病毒变体的疫苗策略,具有特殊的参考意义。
南方医科大学胡方课题组长期致力于有机多功能生物材料、光动力治疗、有机荧光生物材料等方面的研究。基于以上对于快速检测血清中抗SARS-CoV-2 NAbs方法的需求,我校胡方课题组设计并合成了一种具有绿色荧光的聚集诱导发光分子AIE490,并将其包载至聚苯乙烯(PS)微球,通过限制AIE490的分子内运动,获取了一种具有超亮绿色荧光的AIE490纳米微球(AIE490NP),最终设计并构建了一种基于超亮AIE490NP的侧流免疫分析法(LFIA)用于人血清中抗SARS-CoV-2 NAbs的检测,与其他可用于检测抗SARS-CoV-2 Nabs的免疫检测方法相比,该方法具有便携性、快速性、简单性和低成本等优点。与传统的LFIA常使用的胶体金颗粒、量子点微球、镧系元素微球和碳点微球等相比,该方法使用了负载AIE分子的PS微球作为荧光标记物,在这一过程中,PS微球的刚性使得AIE490的分子内运动受到严重抑制,从而触发超亮荧光。在使用临床血清样本进行检测时,该方法可以有效地区分70例COVID-19前的阴性样本与63例来自疫苗接种者的阳性血清(p<0.0001),批内与批间差异分别为6.81-12.99%和7.15-15.03%,有望用于评估新冠疫苗接种者免疫水平及协同指导疫苗免疫策略。该研究成果以“Ultrabright nanoparticle-labeled lateral flow immunoassay for detection of anti-SARS-CoV-2 neutralizing antibodies in human serum”为题发表于Biomaterials 2022(影响因子15.304),第一作者为卞论同学,原文链接:https://doi.org/10.1016/j.biomaterials.2022.121694 。
在该研究中,以典型的AIE单元-四苯乙烯和三苯胺为基础设计并合成了AIE490,进一步构建了AIE490NP(图1A)以及AIE490NP标记的用于检测疫苗接种者及患者血清中抗SARS-CoV-2 NAbs的LFIA,使用AIE490NP作为荧光标记物对ACE2 Fc嵌合体进行修饰(ACE2-AIE490NP);将SARS-CoV-2核衣壳S RBD融合体包被在硝酸纤维素膜上作为检测线。当样品为阴性(不含NAbs)时,由于ACE2-RBD结合力强,检测线呈现出明亮的荧光信号;当样品呈阳性时(含NAbs),由于ACE2-RBD的结合通过NAb-RBD结合受到抑制,检测线呈现出微弱的荧光信号(图1B)。
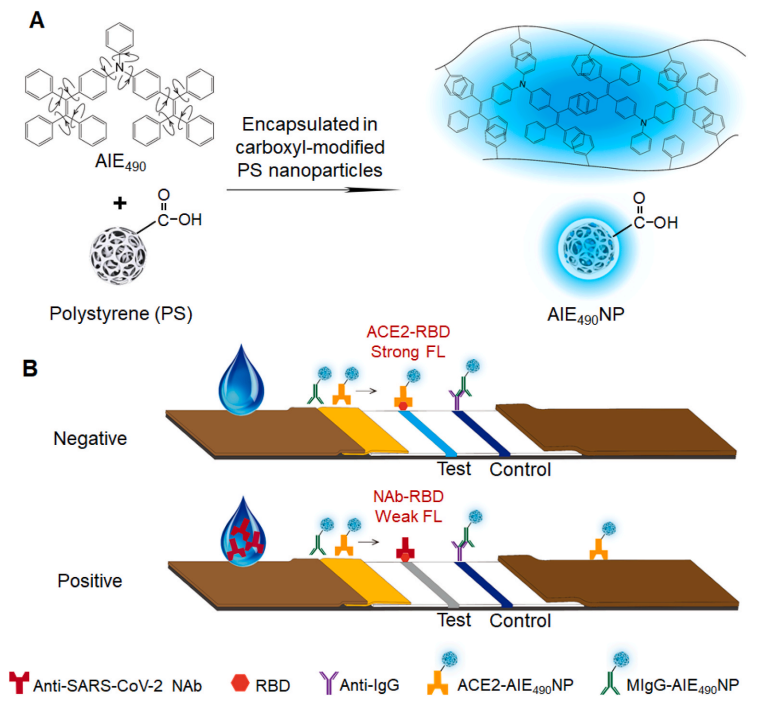
图1 (A)AIE490NP的制备。
(B)开发的基于AIE490NP的LFIA试纸条用于检测人血清样品中的抗SARS-CoV-2 NAbs的示意图。
LFIA产品的图片如图2A所示。包被RBD作为测试线,包被抗IgG作为对照线。将含有人抗SARS-CoV-2 NAb的样品缓冲液滴入样品垫,然后通过毛细作用迁移至偶联垫,并将固定在偶联垫上的AIE490NP-ACE2和AIE490NP-MIgG逐渐带向吸收垫。一旦混合物到达检测线,抗SARS-CoV-2 NAb将与SARS-CoV-2 RBD结合,阻止其识别人ACE2,从而导致检测线的荧光信号(HT)较弱。NAbs浓度越高,荧光信号越弱。同时,抗-IgG和MIgG之间的结合不受影响,因此对照线的荧光信号(HC)不受血清样本中抗-SARS-CoV-2 NAb的干扰。图2B显示了阳性和阴性样品在 365 nm 辐照下的视觉检测结果图片。为了抵消基于AIE490NP的LFIA的内在异质性和血清基质的影响,使用HT和HC的比例作为试纸的最终结果,这将使结果更加可靠和可重复。通过计算抑制率以进一步证实血清样品中NAbs对RBD结合能力的抑制作用。
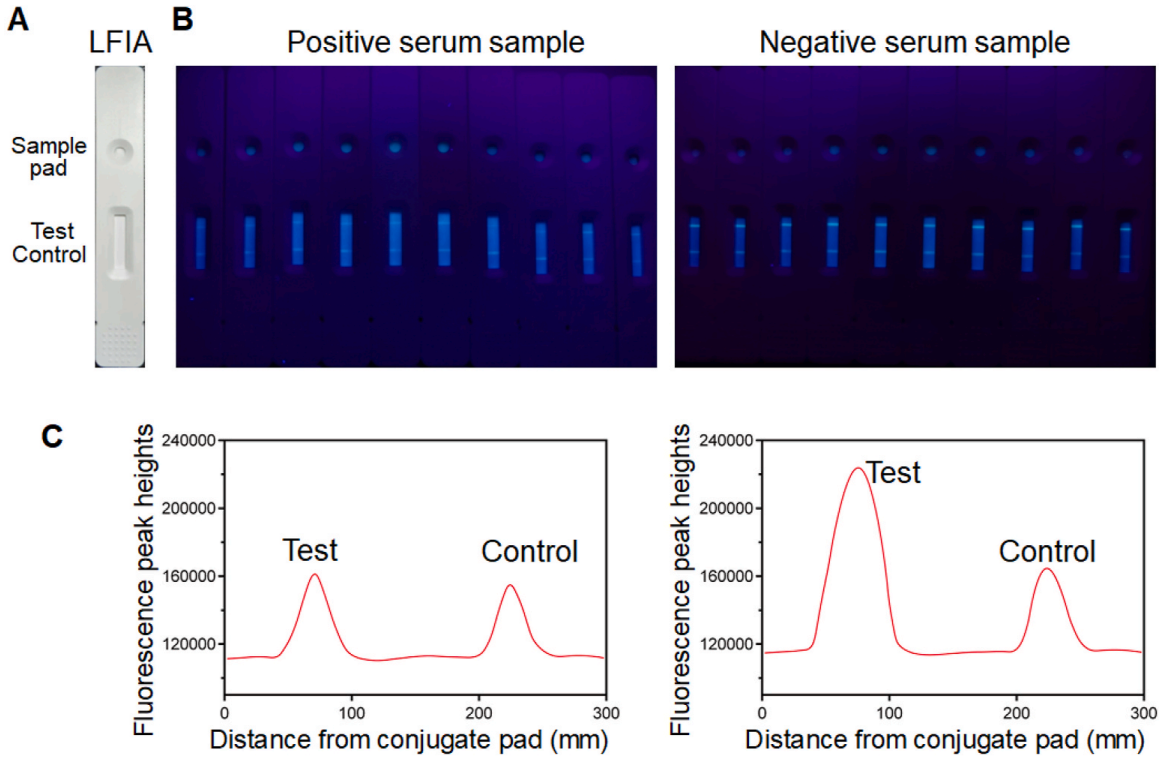
图2 (A)基于AIE490NP的LFIA产品图片。(B)阳性和阴性样品在365 nm照射下的视觉检测结果图片。
(C)阳性样本与阴性样本的荧光峰高读数曲线。
受益于AIE490NP的超亮荧光,使用基于AIE490NP的LFIA准确鉴定了来自疫苗接种者的63份阳性血清样本和70份SARS-CoV-2前血清样本(图3)。
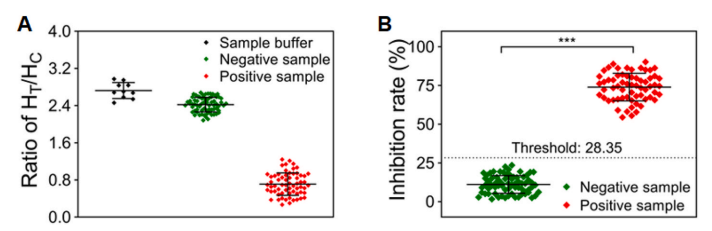
图3 (A)10个样本缓冲液、70个阴性样本和63个阳性样本的HT/HC比率。
(B)70个阴性样本和63个阳性样本的抑制率。虚线表示阈值,计算为阴性样品抑制率的平均值加上3倍标准偏差为28.35。***,p<0.001。